| J Korean Dent Assoc > Volume 62(6); 2024 > Article |
|
Abstract
Ameloblastic fibro-odontoma (AFO) is a rare benign mixed odontogenic tumor predominantly occurring in children. This tumor is often asymptomatic and associated with disturbances in tooth eruption. We present the case of a 7-year-old boy who exhibited delayed eruption of his left mandibular first molar, attributable to AFO with a congenitally missing mandibular second molar. Radiographs revealed a well-defined, ovoid, radiolucent lesion containing sparse calcified materials in the left posterior mandible. To the best of our knowledge, few reports have documented AFO in conjunction with the congenital absence of a permanent tooth. This case is discussed along with a review of relevant literature.
ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņØĆ ņĀĢņāüņĀüņØĖ ņ╣śņĢä ĒśĢņä▒ Ļ│╝ņĀĢ ņżæņŚÉ ņ╣śņä▒ņāüĒö╝ ļ░Å Ļ░äņŚĮ ņĪ░ņ¦üņØ┤ ņØ┤ņāüņ”ØņŗØņØä ĒĢ©ņ£╝ļĪ£ņŹ© ļ░£ņāØļÉśļŖö ņ¢æņä▒ņØś Ēś╝ĒĢ®ņä▒ ņ╣śņä▒ ņóģņ¢æņØ┤ļŗż[1]. ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņØĆ 1967ļģä Hooker [2]Ļ░Ć ļ│æļ”¼ņĪ░ņ¦üĒĢÖņĀü ĒŖ╣ņä▒ņŚÉ ņØśĒĢ┤ ļ▓Ģļ×æļ¬©ņ╣śņĢäņóģņ£╝ļĪ£ļČĆĒä░ ņØ┤ļź╝ ļČäļ”¼ĒĢśņŚ¼ ļ│┤Ļ│ĀĒĢ£ ņØ┤ļל ņ╣śņä▒ņóģņ¢æ ņżæ 3.25% ļ╣äņ£©ļĪ£ Ļ┤Ćņ░░ļÉśĻ│Ā ņ׳ņ£╝ļ®░[3], Chrcanovic [4] ļō▒ņØĆ ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņØś 215 ņé¼ļĪĆļ¦īņØ┤ ļ¼ĖĒŚīņŚÉ ļ│┤Ļ│ĀļÉśņŚłļŗżĻ│Ā ĒĢśņŚ¼ ĒؼĻĘĆĒĢ£ ļ░£ņāØļ╣łļÅäļź╝ ļ│┤ņØ┤ļŖö ņ¦łĒÖśņ×äņØä ņĢī ņłś ņ׳ļŗż.
ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņØĆ ĒĢśņĢģĻ│©ņŚÉņä£ ĒŖ╣Ē׳ ņåīĻĄ¼ņ╣śņÖĆ ļīĆĻĄ¼ņ╣ś ļČĆņ£äņŚÉņä£ ĒśĖļ░£ĒĢśĻ│Ā ļīĆļČĆļČä ņåīņĢäņŚÉņä£ Ļ┤Ćņ░░ļÉśļ®░ ļ░£Ļ▓¼ ĒÅēĻĘĀ ļéśņØ┤ļŖö 9.4ņäĖļĪ£ 20ņäĖ ņØ┤ņāüņŚÉņä£ļŖö ļō£ļ¼╝Ļ▓ī ļéśĒāĆļé£ļŗż[5]. ļ░®ņé¼ņäĀņśüņāüņŚÉņä£ļŖö Ļ▓ĮĻ│äĻ░Ć ļ¬ģĒÖĢĒĢ£ ļŗ©ļ░®ņä▒ņØ┤ļéś ļŗżļ░®ņä▒ ļ│æņåī ļé┤ņŚÉ ņ╣śņĢä Ļ▓ĮņĪ░ņ¦üĻ│╝ ņ£Āņé¼ĒĢ£ ļ░®ņé¼ņäĀ ļČłĒł¼Ļ│╝ņāüņØ┤ Ļ┤Ćņ░░ļÉśļ®░, ņØ┤ļ¤¼ĒĢ£ ļČłĒł¼Ļ│╝ņä▒ ļ¼╝ņ¦łņØś Ēü¼ĻĖ░ņÖĆ ļ░ĆļÅäļŖö ņ”ØļĪĆļ¦łļŗż ļŗżņ¢æĒĢśĻ▓ī ļ│┤Ļ│ĀļÉśĻ│Ā ņ׳ļŗż[6]. ļ▓Ģļ×æļ¬©ņä¼ņ£ĀņóģņØś ņŚ░ņĪ░ņ¦ü ņä▒ļČäĻ│╝ ļ│Ąņ×Īņ╣śņĢäņóģņØś Ļ▓ĮņĪ░ņ¦ü ņä▒ļČäņØ┤ ļÅÖņŗ£ņŚÉ Ļ┤Ćņ░░ļÉśļŖö ņĀÉņØ┤ ņØ┤ ļ│æņåīņØś ļ░®ņé¼ņäĀĒĢÖņĀü ĒŖ╣ņ¦ĢņØ┤ļéś ĻĘĖ ņŗżņ▓┤ņŚÉ ļīĆĒĢ┤ņä£ļŖö ļģ╝ļ×ĆņØ┤ ņ¦ĆņåŹļÉśĻ│Ā ņ׳ļŗż. ņ”ē ļ▓Ģļ×æļ¬©ņä¼ņ£ĀņóģņØ┤ ņŗ£Ļ░ä Ļ▓ĮĻ│╝ņŚÉ ļö░ļØ╝ ļČäĒÖöļÉśļ®┤ņä£ ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņ£╝ļĪ£ ņ¦äĒ¢ēļÉśļ®░, ņĄ£ņóģņĀüņ£╝ļĪ£ ļ│Ąņ×Īņ╣śņĢäņóģņ£╝ļĪ£ ļ░£ļŗ¼ļÉ£ļŗżļŖö ļ│┤Ļ│ĀļōżņØ┤[7] ņ׳ļŖö ļ░śļ®┤ ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņØĆ ļ»Ėņä▒ņłÖļÉ£ ļ│Ąņ×Īņ╣śņĢäņóģņØ┤ļØ╝ļŖö ņŚ░ĻĄ¼ļōż[8,9], ļśÉļŖö ļÅģļ”ĮņĀüņØĖ ņóģņ¢æļ│æņåīļĪ£ņä£ ņĢģĻ│©ļ│ĆĒśĢņØ┤ļéś Ļ│©ĒīīĻ┤┤ļź╝ ņĢ╝ĻĖ░ņŗ£Ēé¼ ņłś ņ׳ļŗżļŖö ņŻ╝ņןļōżņØ┤[10] ņ׳ļŗż.
ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņØĆ ņłĀĒøä ņ×¼ļ░£Ļ▓ĮĒ¢źņØĆ Ļ▒░ņØś ņŚåļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ņ£╝ļ»ĆļĪ£ ņ╣śļŻīļ▓Ģņ£╝ļĪ£ļŖö ņåīĒīīņłĀņØ┤ļéś ņĀüņČ£ņłĀ ļō▒ņØś ļ│┤ņĪ┤ņĀüņØ┤ ļ░®ļ▓ĢņØ┤ ĻČīņןļÉśĻ│Ā ņ׳ņ£╝ļéś, ļ│æņåīĻ░Ć ĒśäņĀĆĒĢśĻ▓ī ņ”ØņŗØĒĢśļŖö Ļ▓ĮņÜ░ņŚÉļŖö Ļ│©ņĀłņĀ£ņłĀ ļō▒ņØ┤ ĒĢäņÜöĒĢĀ ņłśļÅä ņ׳ņ£╝ļ®░[4], ĻĘ╣Ē׳ ļō£ļ¼╝Ļ▓ī ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ£Īņóģņ£╝ļĪ£ņØś ņĢģņä▒ ļ│ĆĒÖöĻ░Ć ļ│┤Ļ│ĀļÉ£ ļ░ö ņ׳ņ£╝ļ»ĆļĪ£ ņŻ╝ņØśĻ░Ć ĒĢäņÜöĒĢśļŗż[11].
ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņØĆ ļ│┤ĒåĄ ļ»Ėļ¦╣ņČ£ņ╣śļéś ļ¦żļ│Ąņ╣śņÖĆ ņŚ░Ļ┤ĆļÉśņ¢┤ ņ╣śņĢäņØś ļ¦╣ņČ£ņןņĢĀļź╝ ņĢ╝ĻĖ░ĒĢ£ļŗżĻ│Ā ļ│┤Ļ│ĀļÉśĻ│Ā ņ׳ņ£╝ļéś[4,9], ņäĀņ▓£ņĀü Ļ▓░ņåÉņ╣śņÖĆ Ļ┤ĆļĀ©ļÉ£ Ļ▓ĮņÜ░ļŖö Ļ▒░ņØś ļ│┤Ļ│ĀļÉśņ¦Ć ņĢŖņĢśļŗż.
Buchner [12] ļō▒ņØ┤ ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģ 114ļĪĆļź╝ ļČäņäØĒĢ£ ņŚ░ĻĄ¼ņŚÉņä£ ĒĢśņĢģ ņĀ£2ļīĆĻĄ¼ņ╣ś ļ░Å ņĀ£3ļīĆĻĄ¼ņ╣ś Ļ▓░ņåÉņØ┤ Ļ┤Ćņ░░ļÉ£ ņ”ØļĪĆļź╝ Ļ░üĻ░ü 1ļĪĆņö® ņĀ£ņŗ£ĒĢ£ ļ│┤Ļ│Āļź╝ ņĀ£ņÖĖĒĢśĻ│ĀļŖö ļ¼ĖĒŚīņāü ņŚ░ĻĄ¼ ļ│┤Ļ│ĀĻ░Ć ņŚåļŗż.
ņ£äņÖĆ Ļ░ÖņØ┤ ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņØĆ ņŻ╝ļĪ£ ņĢäļÅÖ ņĢģĻ│©ņŚÉņä£ ĒؼĻĘĆĒĢśĻ▓ī ļ░£Ļ▓¼ļÉśļŖö ņ¦łĒÖśņ£╝ļĪ£ņä£, ļ░®ņé¼ņäĀĒł¼Ļ│╝ņä▒ ļ│æņåīļé┤ņŚÉ ņäØĒÜīĒÖö ļ¼╝ņ¦łņØ┤ Ēś╝ņ×¼ļÉśņ¢┤ ļéśĒāĆļéśļŖö ĒŖ╣ņ¦ĢņĀüņØĖ ļ░®ņé¼ņäĀĒĢÖņĀü ņåīĻ▓¼ņØä ļéśĒāĆļé┤ļŖö ņ¦łĒÖśņØ┤ļŗż. ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ĒĢśņĢģ ņóīņĖĪ ņĀ£1ļīĆĻĄ¼ņ╣śņØś ņ¦ĆņŚ░ ļ¦╣ņČ£ņØä ņŻ╝ņåīļĪ£ ļé┤ņøÉĒĢ£ ņ¢┤ļ”░ņØ┤ņØś ņóīņĖĪ ņĀ£2ļīĆĻĄ¼ņ╣ś ņäĀņ▓£ņĀü Ļ▓░ņåÉņØ┤ ļ░®ņé¼ņäĀ ņśüņāüņŚÉņä£ ņÜ░ņŚ░Ē׳ ļ░£Ļ▓¼ļÉ£ ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņØś ĒؼĻĘĆ ņ”ØļĪĆļź╝ ļ¼ĖĒŚīĻ│Āņ░░Ļ│╝ ĒĢ©Ļ╗ś ļ│┤Ļ│ĀĒĢśļŖö ļ░öņØ┤ļŗż.
7ņäĖ ļé©ņĢäĻ░Ć ĒĢśņĢģ ņóīņĖĪ ņĀ£1ļīĆĻĄ¼ņ╣śņØś ļ¦╣ņČ£ ņ¦ĆņŚ░ņ£╝ļĪ£ ņ╣śĻ│╝ļ│æņøÉņŚÉ ļé┤ņøÉĒĢśņśĆņ£╝ļ®░ ņłśĻ░£ņøöņĀä ņāüņĢģ ņżæņĀłņ╣śņØś ļ¦╣ņČ£ ņ¦ĆņŚ░ņ£╝ļĪ£ ĒĢ┤ļŗ╣ļČĆņ£ä ņ╣śņØĆ ņĀłņĀ£ņłĀņØä ļ░øņØĆ ņ╣śĻ│╝ņĀü ļ│æļĀź ņÖĖņŚÉļŖö ĒŖ╣ņØ┤ĒĢĀ ļ¦īĒĢ£ ņĀäņŗĀņĀü, ņ╣śĻ│╝ņĀü ļ│æļĀźĻ│╝ Ļ░ĆņĪ▒ļĀźņØĆ ņŚåņŚłļŗż. ĻĄ¼Ļ░Ģļé┤ ņ×äņāü Ļ▓Ćņé¼ņŗ£ ĒĢśņĢģ ņóīņĖĪ ņĀ£2ļīĆĻĄ¼ņ╣ś ļČĆņ£äņŚÉņä£ ņäżņĖĪņ£╝ļĪ£ņØś ļ»ĖņĢĮĒĢ£ ņ╣śņĪ░Ļ│©ņØś ĒīĮņ£ĄņØ┤ ĒāÉņ¦ĆļÉśņŚłņ£╝ļéś ĒÖśņ×É ļ░Å ļ│┤ĒśĖņ×ÉļŖö ņØ┤ļź╝ ņØĖņ¦ĆĒĢśņ¦Ć ļ¬╗ĒĢśĻ│Ā ņ׳ņŚłņ£╝ļ®░ ĒåĄņ”ØņØ┤ļéś ļČłĒÄĖĻ░É ļō▒ ņ¢┤ļ¢ż ņ”ØņāüļÅä Ļ▓ĮĒŚśĒĢśņ¦Ć ņĢŖņĢśļŗżĻ│Ā ĒĢśņśĆļŗż.
ĒīīļģĖļØ╝ļ¦łļ░®ņé¼ņäĀņśüņāü Ļ▓Ćņé¼ņŚÉņä£ ĒĢśņĢģ ņóīņĖĪ ņĀ£2ļīĆĻĄ¼ņ╣śĻ░Ć Ļ▓░ņåÉļÉśņ¢┤ ņ׳ņŚłĻ│Ā, ņ╣śņĢä Ļ▓░ņåÉļČĆņ£äņŚÉ ļé£ĒśĢņØś, Ļ▓ĮĻ│äĻ░Ć ļ¬ģļŻīĒĢ£ ļ░®ņé¼ņäĀ Ēł¼Ļ│╝ņä▒ ļ│æņåīĻ░Ć ļīĆņŗĀ Ļ┤Ćņ░░ļÉśņŚłļŖöļŹ░(ļ│æņåī ņĄ£ļīĆ ņ¦üĻ▓Į 1.5cm) ļ░®ņé¼ņäĀĒł¼Ļ│╝ņä▒ ļ│æņåī ļé┤ļČĆņŚÉļŖö Ēؼļ»ĖĒĢ£ ņäØĒÜīĒÖö ļ¼╝ņ¦łņØ┤ ņåīļ¤ē ņé░ņ×¼ļÉśņ¢┤ ļ│┤ņśĆļŗż. ĻĘĖļ”¼Ļ│Ā ņØ┤ ļ│æņåīņŚÉ ņØśĒĢ┤ ĒĢśņĢģ ņóīņĖĪ ņĀ£1ļīĆĻĄ¼ņ╣śĻ░Ć ņĢĮĻ░ä ņĀäļ░® ļ│Ćņ£äļÉśļ®┤ņä£ ņĀ£2ņ£ĀĻĄ¼ņ╣śņŚÉ ņØśĒĢ┤ ļ¦╣ņČ£ņØ┤ ļ░®ĒĢ┤ļ░øļŖö ņāüņØ┤ Ļ┤Ćņ░░ļÉśņŚłļŗż(Fig. 1). ņĮśļ╣ö CTņŚÉņä£ļŖö Ļ▓ĮĻ│äĻ░Ć ļ¬ģĒÖĢĒĢ£ ļ░®ņé¼ņäĀ Ēł¼Ļ│╝ņä▒ ļ│æņåīņÖĆ ĻĘĖ ļé┤ļČĆņŚÉ ļ░®ņé¼ņäĀ ļČłĒł¼Ļ│╝ņä▒ņØś ļ¼╝ņ¦łļōżņØ┤ Ļ┤Ćņ░░ļÉśņŚłĻ│Ā ļ│æņåīņŚÉ ņØśĒĢ┤ ņäżņĖĪ Ēö╝ņ¦łĻ│©ņØ┤ ņĢĮĻ░ä ļ╣äļ░ĢļÉśĻ│Ā ĒīĮņ£ĄļÉ£ ņāüņØ┤ Ļ┤Ćņ░░ļÉśņŚłļŗż. ņäØĒÜīĒÖö ļ¼╝ņ¦łļōżņØĆ Ēü¼ĻĖ░Ļ░Ć ņ×æĻ│Ā ļ¼┤ņĀĢĒśĢņØ┤ņŚłņ£╝ļ®░, Ēł¼Ļ│╝ņä▒ ļ│æņåī ņżæņŗ¼ ņŻ╝ļ│ĆļČĆņ£äņŚÉ ņé░ņ×¼ļÉśņ¢┤ ņ׳ņŚłļŖöļŹ░, ļ▓Ģļ×æņ¦łĻ│╝ ņ£Āņé¼ĒĢ£ ļ░®ņé¼ņäĀ ļČłĒł¼Ļ│╝ņāüņØ┤ Ļ┤Ćņ░░ļÉśņŚłĻĖ░ ļĢīļ¼ĖņŚÉ ņ╣śņĢäņóģ ņä▒ļČäņØä ņØśņŗ¼ĒĢĀ ņłś ņ׳ņŚłļŗż(Fig. 2. A~C).
ņØ┤ņÖĆ Ļ░ÖņØ┤ ļ░®ņé¼ņäĀĒł¼Ļ│╝ņāüĻ│╝ ļČłĒł¼Ļ│╝ņāüņØ┤ Ēś╝ĒĢ®ļÉ£ ĒŖ╣ņ¦ĢņĀüņØĖ ļ░®ņé¼ņäĀĒĢÖņĀü ņåīĻ▓¼ņØä ļ│┤ņśĆĻĖ░ ļĢīļ¼ĖņŚÉ ņäØĒÜīĒÖöņ╣śņä▒ļéŁ, ņäĀņ¢æņ╣śņä▒ņóģņ¢æ, ņäØĒÜīĒÖöņāüĒö╝ņä▒ņ╣śņä▒ņóģņ¢æ ļō▒ņØś ņĢģĻ│©ļ│æņåīņÖĆ Ļ░Éļ│äņØ┤ ĒĢäņÜöĒĢśņśĆļŗż. ļ│Ė ņ”ØļĪĆņŚÉņä£ļŖö ņäØĒÜīĒÖöļÉ£ ĻĄ¼ņĪ░ļ¼╝ņØ┤ ĒŖ╣ņĀĢĒĢ£ ĒśĢĒā£ļź╝ Ļ░¢ņČöņ¦Ć ņĢŖĻ│Ā ļ░®ņé¼ņäĀ Ēł¼Ļ│╝ņāü ļé┤ņŚÉ ņåīļ¤ē ņé░ņ×¼ļÉśņ¢┤ ņ׳ņŚłņ£╝ļ»ĆļĪ£ ĒŖ╣Ē׳ ņäØĒÜīĒÖöņ╣śņä▒ļéŁĻ│╝ņØś Ļ░Éļ│äņØ┤ ĒĢäņÜöĒĢśņśĆņ£╝ļéś, ļ│æņåī ļ░£Ļ▓¼ņŚ░ļĀ╣ņØ┤ 7ņäĖļĪ£ ņ¢┤ļ”░ ļéśņØ┤ņśĆĻ│Ā ņäØĒÜīĒÖö ļ¼╝ņ¦łņØś ļ░®ņé¼ņäĀ ļČłĒł¼Ļ│╝ ņĀĢļÅäļŖö ņ╣śņĢä Ļ▓ĮņĪ░ņ¦üĻ│╝ ņ£Āņé¼ĒĢśņŚ¼ ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņØä ņČöņĀĢĒĢĀ ņłś ņ׳ņŚłļŗż. ļśÉĒĢ£ ņóīņĖĪ ņĀ£2ļīĆĻĄ¼ņ╣śĻ░Ć Ļ▓░ņåÉļÉśņ¦Ć ņĢŖĻ│Ā ļ░£ņ£ĪņØ┤ ļŹöļöś ļ»Ėņä▒ņłÖĒĢ£ ĒśĢĒā£ļź╝ ņČöņĀĢĒĢĀ ņłśļÅä ņ׳ņŚłņ£╝ļéś, ļ░śļīĆņĖĪņØś ņÜ░ņĖĪ ĒĢśņĢģ ņĀ£2ļīĆĻĄ¼ņ╣śļŖö ņ╣śĻ┤ĆņØ┤ ņØ┤ļ»Ė ĒśĢņä▒ļÉśņ¢┤ ņ׳ļŖö ņāüņØ┤ Ļ┤Ćņ░░ļÉśņŚłņ£╝ļ»ĆļĪ£ ņóīņĖĪ ņĀ£2ļīĆĻĄ¼ņ╣śņØś Ļ▓ĮņÜ░ ņĀĢņāüņĀüņØĖ ņ╣śņĢä ļ░£ņ£ĪĻ│╝ņĀĢņØĆ ņĢäļŗÉ Ļ▓āņØ┤ļØ╝Ļ│Ā ņČöņĀĢĒĢśņśĆļŗż.
ņĪ░ņ¦üļ│æļ”¼ĒĢÖņĀü Ļ▓Ćņé¼Ļ▓░Ļ│╝ ņä¼ņ£Āņä▒ Ļ▓░ĒĢ®ņĪ░ņ¦ü ļ░Å ņ╣śņä▒ ņāüĒö╝, ļ░▒ņĢģņ¦ł ņä▒ļČä ļō▒ņØ┤ Ļ┤Ćņ░░ļÉśņ¢┤ ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņ£╝ļĪ£ ņĄ£ņóģ ņ¦äļŗ©ļÉśņŚłļŗż(Fig. 3). ļ│æņåīļŖö ņåīĒīīņłĀļĪ£ ņĀ£Ļ▒░ļÉśņŚłņ£╝ļ®░ ņŻ╝ņ£ä Ļ▒┤Ļ░Ģ Ļ│©ņĪ░ņ¦üĻ│╝ ņל ļČäļ”¼ļÉśņŚłļŗż. ņłĀĒøä 2Ļ░£ņøöĒøä ņ┤¼ņśüļÉ£ ĒīīļģĖļØ╝ļ¦łļ░®ņé¼ņäĀņśüņāüņŚÉņä£ļŖö ņĀ£2ņ£ĀĻĄ¼ņ╣śņŚÉ ņØśĒĢ£ ĒĢśņĢģ ņóīņĖĪ ņĀ£1ļīĆĻĄ¼ņ╣ś ļ¦╣ņČ£ Ļ▓ĮļĪ£ ņ░©ļŗ©ņØ┤ ņÖäĒÖöļÉśņ¢┤ ļ│┤ņŚ¼ ņĀĢņāüņĀüņØĖ ļ¦╣ņČ£Ļ│╝ņĀĢņØ┤ ĻĖ░ļīĆļÉśņŚłļŖöļŹ░(Fig. 4), ņØ┤ļŖö ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņ£╝ļĪ£ ņØĖĒĢ£ ņĀ£1ļīĆĻĄ¼ņ╣śņØś ņĀäļ░® ļ│Ćņ£äĻ░Ć ļŹö ņØ┤ņāü ņĪ┤ņ×¼ĒĢśņ¦Ć ņĢŖĻĖ░ ļĢīļ¼ĖņŚÉ ņØ╝ņ¢┤ļé£ Ļ▓░Ļ│╝ļØ╝Ļ│Ā ņé¼ļŻīļÉśņŚłļŗż. ņÖĖĻ│╝ņĀü ņłśņłĀļĪ£ ņØĖĒĢ£ Ļ│©Ļ▓░ņåÉļČĆņ£äļŖö ņĀĢņāüņĀüņØĖ ņ╣śņ£Āņ¢æņāüņØä ļ│┤ņØ┤Ļ│Ā ņ׳ņŚłņ£╝ļ®░ ĒĢśņĢģ ņĀ£2ļīĆĻĄ¼ņ╣ś Ļ▓░ņåÉņ£╝ļĪ£ ņØĖĒĢ£ ņóīņĖĪ ņāüņĢģ ņĀ£2ļīĆĻĄ¼ņ╣śņØś ņĀĢņČ£ ļ¼ĖņĀ£ļź╝ ĒĢ┤Ļ▓░ĒĢśĻĖ░ ņ£äĒĢ┤ ĻĄÉņĀĢņ╣śļŻīļź╝ Ļ│äĒÜŹĒĢśļ®┤ņä£ ņłśņłĀļČĆņ£äņØś ņ╣śņ£ĀĻ│╝ņĀĢņØä ņ¦ĆņåŹņĀüņ£╝ļĪ£ Ļ┤Ćņ░░ĒĢśĻĖ░ļĪ£ ĒĢśņśĆļŗż.
ļ│Ė ņ”ØļĪĆļŖö ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņØ┤ ņóīņĖĪ ĒĢśņĢģ ņĀ£2ļīĆĻĄ¼ņ╣ś ļČĆņ£äņŚÉ ļ░£ņāØļÉśļ®┤ņä£ ĒĢ┤ļŗ╣ļČĆņ£ä ņśüĻĄ¼ņ╣śĻ░Ć Ļ▓░ņåÉļÉ£ ļ¦żņÜ░ ĒؼĻĘĆĒĢ£ ņ”ØļĪĆņØ┤ļŗż. ļśÉĒĢ£ ļ░®ņé¼ņäĀ ņśüņāüņŚÉņä£ ļ│æņåī Ēü¼ĻĖ░Ļ░Ć ļ╣äĻĄÉņĀü ņ×æĻ│Ā(ņĄ£ļīĆ ņ¦üĻ▓Į 1.5cm) Ēö╝ņ¦łĻ│© ĒīĮņ£Ąļō▒ņØś ņåīĻ▓¼ņØ┤ ļ»ĖņĢĮĒĢśĻ▓ī Ļ┤Ćņ░░ļÉ£ ņĀÉļÅä ĒŖ╣ņ¦ĢņĀüņØ┤ņŚłņ£╝ļ®░, ļé┤ļČĆ ņäØĒÜīĒÖöļ¼╝ņ¦łļōżņØś Ēü¼ĻĖ░Ļ░Ć ņ×æĻ│Ā ļ│æņåī ņżæņŗ¼ļČĆļź╝ ņżæņŗ¼ņ£╝ļĪ£ ņé░ņ×¼ļÉśņ¢┤ ļ│┤ņśĆļŗż. ņØ┤ļ¤¼ĒĢ£ ņåīĻ▓¼ļōżņØĆ ņØ╝ļČĆ ņäĀĒĢÖļōżņØś ņŚ░ĻĄ¼ņÖĆ ņ£Āņé¼ĒĢ£ ņĀÉņØ┤ļŗż[12]. ĻĘĖļ¤¼ļéś Ļ│ĄĻ▓®ņĀüņØĖ ņ¢æņāüĻ│╝ Ļ│©ĒīĮņ£ĄņØä ĒśäņĀĆĒĢśĻ▓ī ņĢ╝ĻĖ░ņŗ£Ēé© ņ”ØļĪĆļōżļÅä ļ│┤Ļ│ĀļÉśņŚłņ£╝ļ»ĆļĪ£[10] ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņØś ļ░®ņé¼ņäĀĒĢÖņĀü ņåīĻ▓¼ņØ┤ ļŗżņ¢æĒĢ©ņØä ņŗ£ņé¼ĒĢ£ļŗż.
ļ│Ė ņ”ØļĪĆņŚÉņä£ļŖö ĒŖ╣ņ¦ĢņĀüņ£╝ļĪ£ ĒĢśņĢģ ņĀ£2ļīĆĻĄ¼ņ╣śĻ░Ć Ļ▓░ņåÉļÉśņŚłļŗż. ĒĢśņĢģ ņĀ£2ļīĆĻĄ¼ņ╣śņØś ņ╣śĻ┤Ć Ļ▓ĮņĪ░ņ¦üņØś ĒśĢņä▒ņØĆ ņāØĒøä 2.5~3ļģäĻ▓ĮņŚÉ ņŗ£ņ×æļÉśļ®░, ļ▓Ģļ×æņ¦łņØĆ 7~8ļģäņŚÉ ņÖäņä▒ļÉśĻ│Ā, ĻĄ¼Ļ░Ģļé┤ņŚÉļŖö 11~13ņäĖĻ▓ĮņŚÉ ņČ£ĒśäĒĢśļŖö Ļ▓āņØ┤ ņØ╝ļ░śņĀüņØ┤ļŗż[13]. ļ│Ė ņ”ØļĪĆņØś ļ│æņåīļŖö ĒĢśņĢģ ņĀ£2ļīĆĻĄ¼ņ╣śņØś ņ╣śļ░░ ņĪ░ņ¦üņ£╝ļĪ£ļČĆĒä░ ņ£ĀļלļÉ£ Ļ▓āņ£╝ļĪ£ ņé¼ļŻīļÉśļ®░, ĒĢ┤ļŗ╣ ņ╣śņĢäņØś ņ╣śļ░░ ņĪ░ņ¦üņØ┤ ĒśĢņä▒ļÉśļŖö ņŗ£ĻĖ░ņØĖ ņāØĒøä 1~2ņäĖĻ▓ĮļČĆĒä░ ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņ£╝ļĪ£ ļīĆņ╣śļÉśļŖö Ļ│╝ņĀĢņØä Ļ▓¬ņŚłņØä Ļ▓āņ£╝ļĪ£ ņČöņĀĢļÉ£ļŗż[14]. ĻĘĖ ļ░£ņāØņøÉņØĖņŚÉ ļīĆĒĢ┤ņä£ļŖö Ļ░ÉņŚ╝, ņÖĖņāü, ĻĘĖ ņÖĖ ĒŖ╣ļ░£ņä▒ ņÜöņåī ļō▒ņŚÉ ņØśĒĢ┤ ņÖĖļ░░ņŚĮ ļ░Å ņżæļ░░ņŚĮ ņä▒ļČäņØ┤ ņ”ØņŗØĒĢśņŚ¼ ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņØ┤ ļ░£ņāØĒĢ£ļŗżĻ│Ā ļ│┤Ļ│ĀļÉ£ ļ░ö ņ׳ļŗż[15].
ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņØĆ ļ░®ņé¼ņäĀņśüņāüņŚÉņä£ ņŻ╝ņ£ä Ļ▒┤Ļ░ĢĻ│© ņĪ░ņ¦üĻ│╝ņØś Ļ▓ĮĻ│äĻ░Ć ļ¬ģļŻīĒĢśļ®┤ņä£ ļŗ©ļ░®ņä▒ Ēś╣ņØĆ ļŗżļ░®ņä▒ņØä ļéśĒāĆļéśļŖöļŹ░ ļ░®ņé¼ņäĀĒł¼Ļ│╝ņāüņØĆ ņāüĒö╝ ļ░Å Ļ▓░ņ▓┤ņĪ░ņ¦üņØä ļéśĒāĆļé┤ļ®░, ĻĘĖ ļé┤ļČĆņŚÉņä£ļŖö ļŗżņ¢æĒĢ£ Ēü¼ĻĖ░ņÖĆ ĒśĢĒā£ņØś ņäØĒÜīĒÖöļÉ£ ĻĄ¼ņĪ░ļ¼╝ņØ┤ ņé░ņ×¼ļÉśņ¢┤ Ļ┤Ćņ░░ļÉ£ļŗż. ņ”ØļĪĆņŚÉ ļö░ļØ╝ ņäØĒÜīĒÖöļ¼╝ņ¦łņØ┤ Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖļŖö Ļ▓ĮņÜ░ņŚÉļŖö ļ¦żļ│Ąņ╣śņÖĆ ņŚ░Ļ┤ĆļÉ£ ĒĢ©ņ╣śņä▒ ļéŁņóģņ£╝ļĪ£ ņśżņ¦äļÉĀ ņłś ņ׳ļŗż[9].
ļ░®ņé¼ņäĀĒł¼Ļ│╝ņä▒ ļČĆņ£äļé┤ņŚÉ ņäØĒÜīĒÖöļ¼╝ņ¦łņØ┤ ņåīļ¤ēņØ╝ Ļ▓ĮņÜ░ņŚÉļŖö ĒŖ╣Ē׳ ņäØĒÜīĒÖöņ╣śņä▒ļéŁ, ņäĀņ¢æņ╣śņä▒ņóģņ¢æ ļō▒Ļ│╝ņØś Ļ░Éļ│äņØä ņÜöĒĢ£ļŗż[16]. ņäØĒÜīĒÖöņ╣śņä▒ļéŁņØĆ 10~20ļīĆ ņĀŖņØĆ ņŚ░ļĀ╣ņĖĄ Ēś╣ņØĆ 50~60ļīĆņØś ļŗżņåī Ļ│ĀļĀ╣ņĖĄņŚÉņä£ ĒśĖļ░£ ļÉ£ļŗżĻ│Ā ļ│┤Ļ│ĀļÉśĻ│Ā ņ׳ņ£╝ļ®░ ļéŁņä▒ ņĪ░ņ¦üĻ│╝ ņóģņ¢æ ņĪ░ņ¦üņØ┤ ļÅÖņŗ£ņŚÉ Ļ┤Ćņ░░ļÉśļŖö Ļ▓ĮņÜ░ļÅä ļ¦ÄĻ│Ā ļŗżņ¢æĒĢ£ ņĪ░ņ¦ü ņåīĻ▓¼ņØä ļ│┤ņØĖļŗż[16]. ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņØś Ļ▓ĮņÜ░ ņäØĒÜīĒÖöļ¼╝ņ¦łņØ┤ ļ│Ąņ×Īņ╣śņĢäņóģņØś ņä▒ļČäņØĖ ņ╣śņĢä Ļ▓ĮņĪ░ņ¦üņ£╝ļĪ£ ĻĄ¼ņä▒ļÉśļŖöļŹ░ ļ╣äĒĢ┤ ņäØĒÜīĒÖöņ╣śņä▒ļéŁņØś Ļ▓ĮņÜ░ ņ╣śņĢä Ļ▓ĮņĪ░ņ¦ü ņä▒ļČä ļ│┤ļŗżļŖö ņ£ĀļĀ╣ ņäĖĒżļĪ£ ņĢīļĀżņ¦ä Ļ░üĒÖöļÉśĻ│Ā ņäØĒÜīĒÖöļÉ£ ņāüĒö╝ņäĖĒżņØś ņĪ┤ņ×¼ļĪ£ ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģĻ│╝ Ļ░Éļ│äĒĢĀ ņłś ņ׳ļŗż. ĻĘĖļ¤¼ļéś ņäØĒÜīĒÖöņ╣śņä▒ļéŁņØĆ ĻĘĖ Ēæ£Ēśäņ¢æņŗØņØ┤ ļŗżņ¢æĒĢśļ»ĆļĪ£ ņ╣śņĢäņóģĻ│╝ ņŚ░Ļ┤ĆļÉ£ ņ”ØļĪĆņØĖ Ļ▓ĮņÜ░ņŚÉļŖö Ļ░Éļ│äņØ┤ ņēĮņ¦Ć ņĢŖņØä ņłś ņ׳ļŗż[17]. ņäĀņ¢æņ╣śņä▒ņóģņ¢æņØĆ 10ļīĆņŚÉņä£ ĒśĖļ░£ĒĢśļ®░ ņĀäņ╣śļČĆ ņżæ ĒŖ╣Ē׳ ņāüņĢģ ņĀäņ╣śļČĆĻ░Ć ĒśĖļ░£ļČĆņ£äņØ┤ļŗż[18]. ņäĀņ¢æņ╣śņä▒ņóģņ¢æ ļé┤ ņäØĒÜīĒÖö ļ¼╝ņ¦łņØś ņĀĢņ▓┤ļŖö ļ»Ėņä▒ņłÖļÉ£ ļ▓Ģļ×æņ¦ł, ņāüņĢäņ¦łņāü, ļ░▒ņĢģņ¦ł ļō▒ņØ┤ļ®░ ņĀÉņāü ĒśĢĒā£ņØś ņäØĒÜīĒÖöļ¼╝ņ¦łņØ┤ ļ│┤Ļ│ĀļÉśĻĖ░ļÅä ĒĢśņśĆļŗż[18]. ĻĘĖ ņÖĖņŚÉļÅä ļ▓Ģļ×æļ¬©ņä¼ņ£ĀņāüņĢäņóģĻ│╝ņØś Ļ░Éļ│äņØ┤ ĒĢäņÜöĒĢĀ ņłśļÅä ņ׳ļŗż. Hisazumi [19] ļō▒ņØ┤ ļ│┤Ļ│ĀĒĢ£ ĒĢśņĢģ ņĀ£2ņåīĻĄ¼ņ╣śļČĆņ£äņØś ļ▓Ģļ×æļ¬©ņä¼ņ£ĀņāüņĢäņóģņØś ņ”ØļĪĆņŚÉņä£ļŖö ņ╣śļ░░ ĻĄ¼ņĪ░ļéś ļ▓Ģļ×æņ¦ł ļō▒ņØś ņä▒ļČäņØĆ ļ░£Ļ▓¼ļÉśņ¦Ć ņĢŖņĢśĻ│Ā ņśżņ¦ü ņāüņĢäņ¦ł Ļ┤ĆļĀ© ņĪ░ņ¦üļ¦ī Ļ┤Ćņ░░ļÉśņŚłĻ│Ā ņØ┤ļ¤¼ĒĢ£ ņĀÉņŚÉņä£ ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģĻ│╝ ļ▓Ģļ×æļ¬©ņä¼ņ£ĀņāüņĢäņóģņØ┤ ņāØĻ▓Ćņāüņ£╝ļĪ£ ĻĄ¼ļ│äļÉĀ ņłś ņ׳ļŗżĻ│Ā ņé¼ļŻīļÉśņŚłļŗż.
ļ░®ņé¼ņäĀļČłĒł¼Ļ│╝ņä▒ ļČĆņ£äņØś ļ╣äņ£©ņØ┤ ņāüļīĆņĀüņ£╝ļĪ£ Ēü░ ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģ ņé¼ļĪĆļÅä ļ│┤Ļ│ĀļÉ£ ļ░öļÅä ņ׳ņ£╝ļ®░[10] ņØ┤ļ¤░ Ļ▓ĮņÜ░ļŖö ņ╣śņĢäņóģĻ│╝ņØś Ļ░Éļ│äņØ┤ ĒĢäņÜöĒĢ£ļŗż. ĒŖ╣Ē׳ ļ│Ąņ×Īņ╣śņĢäņóģņØĆ Ēøäļ░® ĻĄ¼ņ╣śņŚÉņä£ ļ╣äĻĄÉņĀü ĒØöĒĢśĻ▓ī Ļ┤Ćņ░░ļÉśĻ│Ā ļ¦żļ│Ąņ╣śņÖĆ Ļ┤ĆļĀ©ļÉśņ¢┤ Ļ┤Ćņ░░ļÉśĻĖ░ ļĢīļ¼ĖņŚÉ ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģĻ│╝ņØś Ļ░Éļ│äņØä ņÜöĒĢ£ļŗż[14]. ĻĘĖļ¤¼ļéś ļ│Ąņ×Īņ╣śņĢäņóģņŚÉņä£ļŖö ņ╣śņĢä Ļ▓ĮņĪ░ņ¦üņØś ļ░®ņé¼ņäĀļČłĒł¼Ļ│╝ņä▒ ļČĆņ£äĻ░Ć ļīĆļČĆļČäņØś ņśüņŚŁņ£╝ļĪ£ Ļ┤Ćņ░░ļÉśĻ│Ā, ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņØś Ļ▓ĮņÜ░ņŚÉļŖö ņāüĒö╝ ļ░Å Ļ▓░ņ▓┤ņĪ░ņ¦üņØś ņŚ░ņĪ░ņ¦ü ļČĆņ£äĻ░Ć ņāüļīĆņĀüņ£╝ļĪ£ ļ¦ÄĻĖ░ ļĢīļ¼ĖņŚÉ ļ░®ņé¼ņäĀĒł¼Ļ│╝ņä▒ļČĆņ£äĻ░Ć ļ│Ąņ×Īņ╣śņĢäņóģņŚÉ ļ╣äĒĢ┤ņä£ ņāüļīĆņĀüņ£╝ļĪ£ ļ¦ÄņØĆ ņĀÉņØ┤ Ļ░Éļ│äņĀÉņØ┤ļŗż[6].
ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņØś ņŗżņ▓┤ņŚÉ ļīĆĒĢ┤ņä£ļŖö ņśżļ×½ļÅÖņĢł ļģ╝ļ×ĆņØä Ļ▒░ļōŁĒĢśņśĆņ£╝ļ®░, ĒؼņåīĒĢ£ ņ”ØļĪĆļ│┤Ļ│ĀņÖĆ ņןĻĖ░ņĀüņØĖ ņČöņĀüĻ┤Ćņ░░ņØś ņ¢┤ļĀżņøĆ ļĢīļ¼ĖņŚÉ ņŗżņ▓┤ ņ×ģņ”ØņŚÉ ļīĆĒĢ£ ņŚ░ĻĄ¼ņØś ņ¢┤ļĀżņøĆņØ┤ ļ¦Äļŗż. Buchner [12] ļō▒ņØĆ ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģ 114 ņ”ØļĪĆļź╝ ļČäņäØĒĢ£ Ļ▓░Ļ│╝ ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģ ņØ╝ļČĆļŖö Ļ│╝ņśżņóģ ņä▒Ļ▓®ņØś ņ╣śņĢäņóģņ£╝ļĪ£ņØś ļ░£ņĀäĒĢ┤ ļéśĻ░ĆļŖö ļŗ©Ļ│äļØ╝Ļ│Ā ņČöņĀĢĒĢĀ ņłś ņ׳ņ£╝ļéś, ņ╣śņĢäņóģņØ┤ ņĢäļŗī ņóģņ¢æņØś ņä▒Ļ▓®ņØä ļ│┤ņØ┤ļŖö ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģĻ│╝ņØś Ļ░Éļ│äņØ┤ ļ│æļ”¼ņĪ░ņ¦üĒĢÖņĀüņ£╝ļĪ£ Ļ░ĆļŖźĒĢśņ¦Ć ņĢŖĻĖ░ ļĢīļ¼ĖņŚÉ ļ░®ņé¼ņäĀĒĢÖņĀü ņ×äņāüņĀü ĒŖ╣ņ¦ĢļōżņØ┤ ņØ┤ļōż ļ│æņåīļōżņØä Ļ░Éļ│äĒĢśļŖöļŹ░ ļÅäņøĆņØä ņżä ņłś ņ׳ļŗżĻ│Ā ĒĢśņśĆļŗż. ņ╣śņĢäņóģņØĆ ņØ╝ņĀĢņŗ£ĻĖ░ņŚÉ ļÅäļŗ¼ĒĢśļ®┤ ļŹö ņØ┤ņāü ņä▒ņןĒĢśņ¦Ć ņĢŖĻĖ░ ļĢīļ¼ĖņŚÉ ņśłĒøäĻ░Ć ļ¦żņÜ░ ņóŗņØĆ ĒÄĖņØ┤ļéś, ņóģņ¢æņØś ņä▒Ļ▓®ņØä Ļ░Ćņ¦ĆļŖö ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņØś Ļ▓ĮņÜ░ ļ│æņåīĻ░Ć Ļ│äņåŹ ņä▒ņןĒĢśņŚ¼ ņØĖņĀæņĪ░ņ¦üņØä ņ╣©ļ▓öĒĢśĻ▒░ļéś ņŗ¼ĒĢ£ ņĢłļ¬©ļ│ĆĒśĢņØä ņĢ╝ĻĖ░ĒĢĀ ņłś ņ׳ĻĖ░ ļĢīļ¼ĖņŚÉ ļ│æņåīņØś ņŗżņ▓┤ ĻĘ£ļ¬ģņØĆ ļ│æņåīņØś ņ╣śļŻī ļ░Å ņśłĒøä Ļ▓░ņĀĢņŚÉ ņżæņÜöĒĢ£ ļ│ĆņłśĻ░Ć ļÉĀ ņłś ņ׳ļŗżĻ│Ā ņé¼ļŻīļÉ£ļŗż.
ļ│Ė ņ”ØļĪĆļŖö ļ│æņåī Ēü¼ĻĖ░Ļ░Ć ņ×æĻ│Ā Ēö╝ņ¦łĻ│© ĒīĮņ£ĄņØ┤ ļ¦żņÜ░ ļ»ĖņĢĮĒĢśņśĆĻĖ░ ļĢīļ¼ĖņŚÉ ņóģņ¢æņØś ņ┤łĻĖ░ ļŗ©Ļ│ä Ēś╣ņØĆ ļ»Ėņä▒ņłÖļŗ©Ļ│äņØś ņ╣śņĢäņóģ ļō▒ņØś ĒĢ┤ņäØņØ┤ ļ¬©ļæÉ Ļ░ĆļŖźĒĢśņśĆļŗż. ĻĘĖļ¤¼ļéś ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņ£äņØś ļģ╝ļ×ĆņØ┤ ņĪ┤ņ×¼ĒĢ©ņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā ņāØĻ▓Ć Ļ▓░Ļ│╝ņŚÉ ĻĖ░ļ░śĒĢ£ ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņ£╝ļĪ£ ņĄ£ņóģ ņ¦äļŗ©ĒĢśņśĆļŗż. ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņØĆ ļ│æņåīĻ░Ć ņל Ēö╝ļ¦ēĒÖö ļÉśņ¢┤ ņ׳Ļ│Ā ĻĄŁņåīņĀü ņ╣©ņŖĄņØä ĒĢśņ¦Ć ņĢŖĻĖ░ ļĢīļ¼ĖņŚÉ ļŗ©ņł£ĒĢ£ ņåīĒīīņłĀņØ┤ļéś ņĀüņČ£ņłĀņØ┤ ņŗ£Ē¢ēļÉ£ļŗżĻ│Ā ļ│┤Ļ│ĀļÉśņŚłņ£╝ļ®░ ļ│Ė ņé¼ļĪĆņŚÉņä£ļÅä ļ│æņåīļŖö ļŗ©ņł£ ņåīĒīīņłĀļĪ£ ņĀ£Ļ▒░ļÉśņŚłļŗż.
ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģņØĆ ņĢäļÅÖ ļ░Å ņ¢┤ļ”░ņØ┤ņŚÉņä£ ņŻ╝ļĪ£ ļ░£Ļ▓¼ļÉśļŖöļŹ░, Philipsen [9] ļō▒ņØ┤ 1997ļģäņŚÉ ļ│┤Ļ│ĀĒĢ£ ļ▓Ģļ×æļ¬©ņä¼ņ£Āņ╣śņĢäņóģ 86ņé¼ļĪĆ ņżæ ļŗ© 1ņé¼ļĪĆļ¦īņØ┤ 20ņäĖ ņØ┤ņāüņØ┤ņŚłņ£╝ļ®░ ļīĆĻ░£ ļ»Ėļ¦╣ņČ£ņ╣śņÖĆ ņŚ░Ļ┤ĆļÉśņ¢┤ ņ׳ņŚłļŗż. Hooker [2]ļŖö ļ│æņåī ļ░£Ļ▓¼ ņŚ░ļĀ╣ņØ┤ ĒÅēĻĘĀ 11.5ņäĖļØ╝Ļ│Ā ĒĢśņśĆĻ│Ā, Slootweg [8]ļŖö ĒÅēĻĘĀ 8.1ņäĖļź╝ ļ│┤Ļ│ĀĒĢśņśĆņ£╝ļ®░, ļ│Ė ĒÖśņ×ÉņØś Ļ▓ĮņÜ░ ņäĀĒĢÖļōżņØś ļ│┤Ļ│Āļ│┤ļŗż ņ¢┤ļ”░ 7ņäĖņśĆļŗż. ņä▒ļ│äņŚÉ ļö░ļźĖ ņ░©ņØ┤ļŖö Ļ▒░ņØś ņŚåļŗżĻ│Ā ĒĢśņśĆņ£╝ļéś Hooker [2]ļŖö 3 : 1ļĪ£ ļé©ņä▒ņŚÉņä£ ņĢĮĻ░ä ļŹö ĒśĖļ░£ĒĢ£ļŗżĻ│Ā ĒĢśņśĆļŗż. ļśÉĒĢ£ ņāüņĢģļ│┤ļŗżļŖö ĒĢśņĢģņŚÉņä£, ņĀäņ╣śļČĆļ│┤ļŗżļŖö Ēøäļ░®ĻĄ¼ņ╣śļČĆņŚÉņä£ ĒśĖļ░£ļÉ£ļŗżĻ│Ā ņĢīļĀżņĀĖ ņ׳ļŗż[9].
ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļŖö 7ņäĖ ļé©ņĢäņØś ĒĢśņĢģ ņĀ£2ļīĆĻĄ¼ņ╣śĻ░Ć Ļ▓░ņåÉļÉ£ ļČĆņ£äņŚÉņä£ ļ▓Ģļ×æņĢäņä¼ņ£Āņ╣śņĢäņóģņØ┤ ļ»ĖņĢĮĒĢśĻ▓ī ņä▒ņןļÉśļŖö ņ”ØļĪĆļź╝ ļ│┤Ļ│ĀĒĢśņśĆņ£╝ļ®░, ļ│Ė ņ”ØļĪĆļŖö ļ▓Ģļ×æņĢäņä¼ņ£Āņ╣śņĢäņóģņØś ļŗżņ¢æĒĢ£ ņ×äņāü ļ░Å ļ░®ņé¼ņäĀĒĢÖņĀü ĒŖ╣ņ¦ĢļōżņØä ņŚ░ĻĄ¼ĒĢśļŖöļŹ░ ņØ╝ļČĆ ņ×ÉļŻīļĪ£ ĒÖ£ņÜ®ļÉĀ Ļ▓āņ£╝ļĪ£ ĻĖ░ļīĆļÉ£ļŗż.
ACKNOWLEDGEMENTS
ļ│Ė ņŚ░ĻĄ¼ļŖö 2024ĒĢÖļģäļÅä ņøÉĻ┤æļīĆ ĻĄÉļ╣äņŚ░ĻĄ¼ļ╣äņØś ņ¦ĆņøÉņŚÉ ņØśĒĢ┤ ņ¦äĒ¢ēļÉśņŚłņØī.
Figure┬Ā1.
Panoramic radiograph displays a well-defined, ovoid, radiolucent lesion with a few calcified materials in the left mandibular posterior region of the absent second molar. The second molar is congenitally absent. The eruption of the first molar appears anteriorly displaced by this lesion, and its eruption is obstructed by the second primary molar.
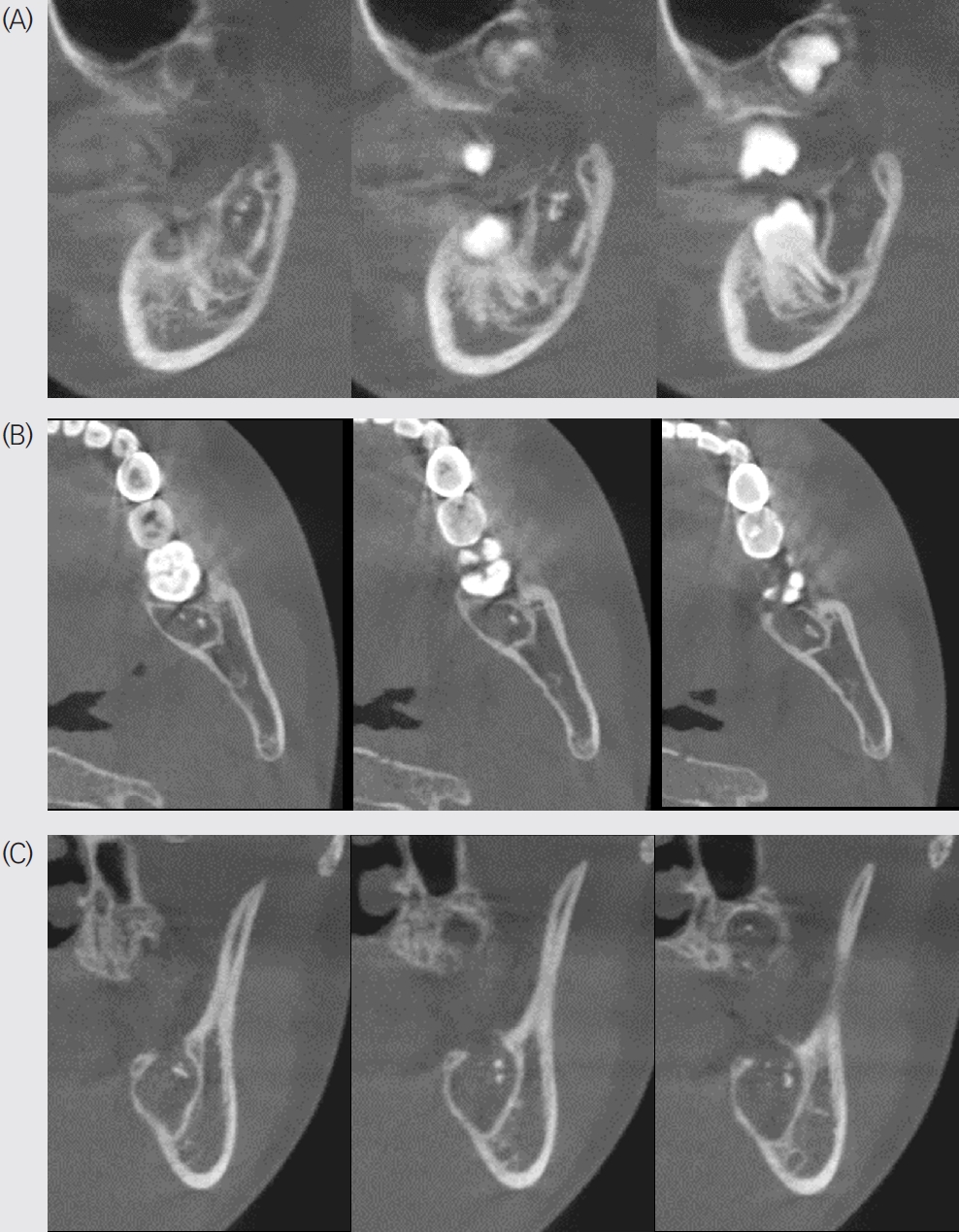
Figure┬Ā2.
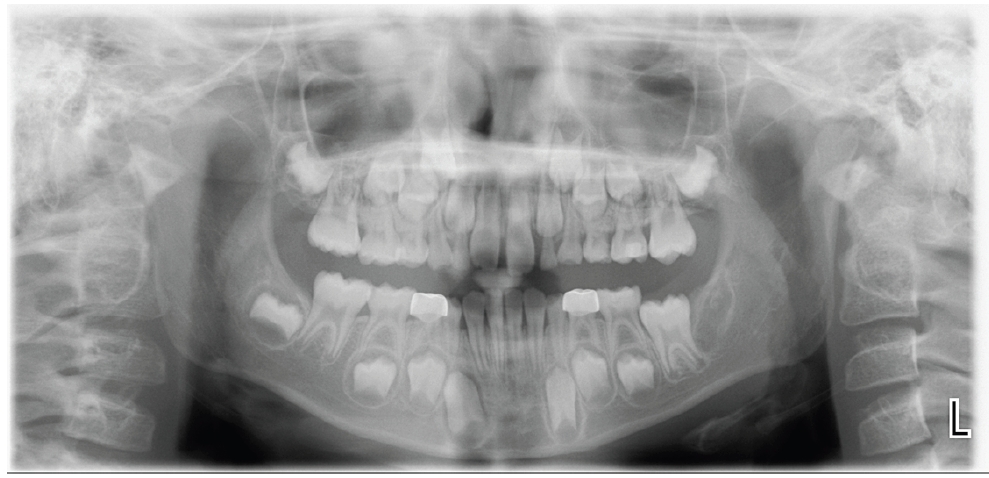
Cone beam CT images provide a detailed view of the calcified materials and cortical alteration in the area of the missing mandibular second molar. Sagittal (A) and axial (B) views reveal amorphous, scattered calcified materials within a unilocular, radiolucent lesion with well-defined borders, exhibiting radiopacity similar to tooth structure. The coronal image (C) shows a corticated border of the lesion with slight expansion and thinning of the lingual cortex.
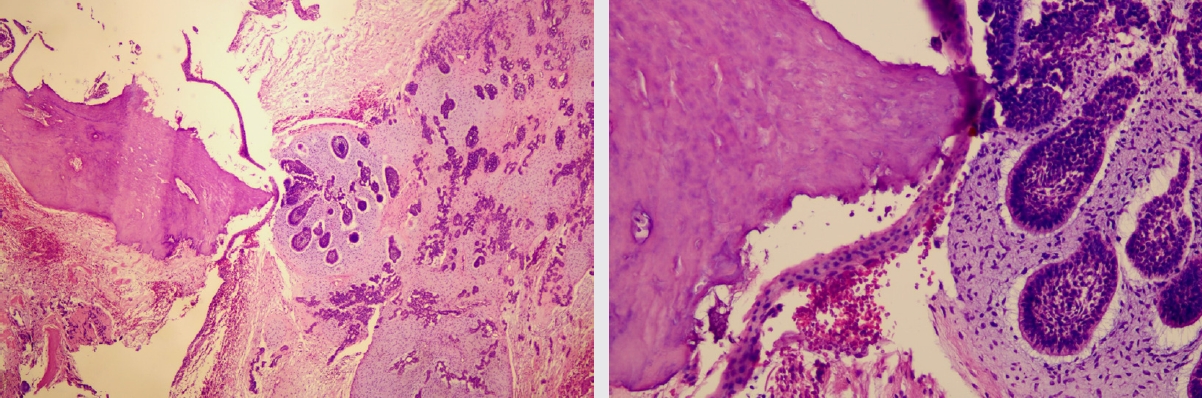
Figure┬Ā3.
Histopathologic images present reduced enamel epithelium, cementum, and odontogenic epithelial islands (stained with hematoxylin and eosin).
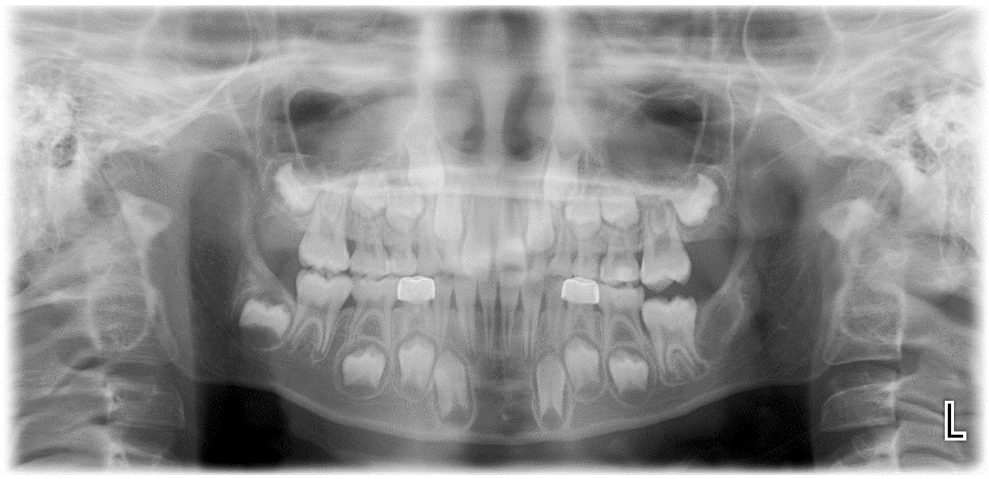
Figure┬Ā4.
Panoramic radiograph from a two-month postoperative follow-up shows the surgical defect without calcified material and an enhanced eruption pattern of the left mandibular first molar, compared with the preoperative image (Figure 1).
REFERENCES
1. Barnes L, Eveson JW, Reichart P, Sidransky D. World Health Organization classification of tumours: pathology and genetics of head and neck tumours. IARC. 2005.
3. Soluk-Tekkesin M, Cakarer S, Aksakalli N, Alatli C, Olgac V. New World Health Organization classification of odontogenic tu┬Łmours: impact on the prevalence of odontogenic tumours and analysis of 1231 cases from Turkey. Br J Oral Maxillofac Surg 2020;58(8):1017ŌĆō22.


4. Chrcanovic BR, Gomez RS. Ameloblastic fibrodentinoma and Ameloblastic fibro-odontoma: an updated systematic review of cases reported in the literature. J Oral Maxillofac Surg 2017;75(7):1425ŌĆō37.


5. Soluk-Tekkesin M, Vered M. Ameloblastic Fibro-Odontoma: At the Crossroad Between ŌĆ£Developing OdontomaŌĆØ and True Odontogenic Tumour. Head Neck Pathol 2021;15(4):1202ŌĆō1211.



6. Langlais RP, Langland OE, Nortje CJ. Diagnostic Imaging of the Jaws. Michigan: Williams & Wilkins, 1995.
7. Barnes L. Surgical Pathology of the Head and Neck. 3rd ed. India: Informa, 2009.
8. Slootweg PJ. An analysis of the interrelationship of the mixed odontogenic tumors.ameloblastic fibroma, ameloblastic fibro-odontoma, and the odontomas. Oral Surg Oral Med Oral Pathol 1981;51(3):266ŌĆō276.


9. Philipsen HP, Reichart PA, Pratorius F. Mixed odontogenic tu┬Łmors and odontomas: Considerations on interrelationship. Review of the literature and presentation of 134 new cases of odontomas. Review of the literature and presentation of 134 new cases of odontomas. Oral Oncol 1997;33(2):86ŌĆō99.
10. Pillai A, Moghe S, Guru KN, Nair PP. Large ameloblastic fibro-odontoma in an 18-year-old girl and review of literature. BMJ Case Rep 2012;19:bcr-2012-007160.



11. Shadavlonjid B, Cho E, Nam W, Kim HS, Yook JI, Kim J. A case of ameloblastic fibrosarcoma transformed from ameloblastic fibro-odontoma. Korean J Oral Maxillofac Pathol 2017;41(1):45ŌĆō50.

12. Buchner A, Kaffe I, Vered M. Clinical and radiological profile of ameloblastic fibro-odontoma: an update on an uncommon odontogenic tumor based on a critical analysis of 114 cases. Head Neck Pathol 2013;7(1):54ŌĆō63.


13. ļīĆĒĢ£ņåīņĢäņ╣śĻ│╝ĒĢÖĒÜī. ņåīņĢäņ▓Łņåīļģäņ╣śĻ│╝ĒĢÖ. ņĀ£6ĒīÉ. ņä£ņÜĖ:ļīĆĒĢ£ļéśļלņČ£ĒīÉņé¼; 2023.
14. Nolla C. The development of permanent teeth (Dissertation). Univ Mich. Published online 1952.
15. Cohen DM, Bhattacharyya I. Ameloblastic fibroma, ameloblastic fibro-odontoma, and odontoma. Oral Maxillofac Surg Clin N Am 2004;16(3):375ŌĆō384.

16. Phillips MD, Closmann JJ, Baus MR, Torske KR, Williams SB. Hybrid odontogenic tumor with features of ameloblastic fibroodontoma, Calcifying Odontogenic Cyst, and Adenomatoid Odontogenic Tumor: A Case Report and Review of the Literature. J Oral Maxillofac Surg 2010;68(2):470ŌĆō474.


17. Samir MC, Lamiae G, Bassima C. Calcifying odontogenic cyst of anterior maxillary: Case report and review. Int J Surg Case Rep 2021;85:106267.



18. Zeitoun IM, Dhanrajani PJ, Mosadomi HA. Adenomatoid odontogenic tumor arising in a calcifying odontogenic cyst. J Oral Maxillofac Surg 1996;54(5):634ŌĆō637.


19. Hisazumi I, Tokutarou M, Shuichi F, Izumi A. Ameloblastic fi┬Łbrodentinoma with a congenitally missing second premolar tooth: a case report. Oral Surg Oral Med Oral Pathol Oral Radiol 2014;117:88ŌĆō91.
-
METRICS

-
- 0 Crossref
- 0 Scopus
- 590 View
- 10 Download
- ORCID iDs
-
Yu Ri Kim

https://orcid.org/0009-0006-0450-1517Byung-Do Lee

https://orcid.org/0000-0002-1660-7339 - Related articles



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print