치성 감염으로부터 유발된 두경부 괴사성 근막염의 진행 중 안와 침범을 동반한 증례 보고
Orbital involvement during the progression of cervicofacial necrotizing fasciitis originating from an odontogenic infection: A case report
Article information
Trans Abstract
Necrotizing fasciitis of the head and neck is a rare but potentially fatal infection that often arises from odontogenic sources and can rapidly spread along fascial planes to adjacent vital structures. We report a case of a 62-year-old male with diabetes who developed odontogenic necrotizing fasciitis originating from the left mandibular premolar region, which progressed to involve the ophthalmic area. Despite initial incision and drainage with intravenous antibiotics, the infection rapidly advanced with fistula formation and extensive necrosis. The patient underwent repeated debridement, vacuum-assisted closure therapy, and subsequently wide surgical excision followed by reconstructive procedures including a split-thickness skin graft and a pectoralis major flap. With timely multidisciplinary management and strict glycemic control, the patient achieved favorable recovery without recurrence.
서론
괴사성 근막염(necrotizing fasciitis)은 근막과 피하조직을 침범하는 급속 진행성 감염으로, 광범위한 조직괴사와 심한 전신 독성을 특징으로 하며 높은 사망률을 보이는 치명적인 질환이다[1]. 특히 두경부에 발생한 괴사성 근막염은 두경부의 심한 통증, 발적, 염증, 부종, 그리고 혈관 압박 혹은 허혈성 괴사로 이어지는 혈전증 등이 발생할 수 있으며, 다른 괴사성 연조직 감염과 달리 주변 조직으로 급속히 확산된다는 점이 특징적이다[2]. 심하게는 Ludwig angina, 경동맥의 국소적 조직결손(carotid artery erosion), 종격동염(descending mediastinitis), Lemierre’s syndrome이라고 불리는 내경정맥의 혈전정맥염(internal jugular vein thrombophlebitis)으로까지 이어질 수 있다[3]. 괴사성 근막염의 두경부 영역에서 발생은 상대적으로 드문데, 전체 괴사성 근막염 중 두경부 괴사성 근막염이 차지하는 비율은 약 5.3% 정도로 보고된다[4]. 그러나 앞서 언급하였다시피 발생 빈도는 낮으나 해부학적으로 기도, 주요 혈관, 종격동과 인접해 있어 임상적 위험도는 매우 크다.
두경부 괴사성 근막염의 주요 원인은 치성(odontogenic) 감염으로, 여러 체계적 고찰에 따르면 약 40~47%가 치성 감염에서 기원하는 것으로 보고되었다[5,6]. 그 외에도 편도주위 감염, 외상, 악성종양, 침습적 시술 등이 원인이 될 수 있다. 특히 두경부 괴사성 근막염은 해부학적 특성상 감염이 빠르게 확산되는 경향이 있으며, 일부 보고에서는 안면부로의 확산이 약 22%, 하경부로의 확산이 약 56%, 종격동으로의 확산이 약 40%에 이른다고 한다[7]. 이처럼 두경부 괴사성 근막염은 초기 국소 감염에서 시작되더라도 단기간 내에 광범위한 파급과 전신적 합병증을 초래할 수 있어 조기 진단과 적극적인 외과적 처치가 필수적이다. 또한, 두경부 괴사성 근막염 환자 대부분은 당뇨병, 알코올 중독, 만성 신부전, 스테로이드 장기 사용 등 면역 저하 상태와 같은 기저질환을 가지고 있으며[8], 이러한 동반질환은 질환의 발생 위험뿐 아니라 예후에도 큰 영향을 준다. 실제로 당뇨 환자에서 괴사성 근막염의 발생 빈도가 높고 사망률 또한 상승한다는 보고가 다수 있다[9]. 또한 최근 보고에 따르면 일부 환자에서는 선천면역 관련 유전자(NFKB1, TLR 등)의 변이나 특정 HLA 대립유전자가 괴사성 근막염 발생 위험을 높일 수 있음이 제시되고 있다[10]. 이러한 관점은 전신적 기저질환 외에도 개체의 유전적 배경을 고려할 필요성을 보여준다.
본 증례의 환자는 당뇨를 기저질환으로 가지며, 본원 내원 3년전 우측 하지의 괴사성 근막염으로 절제술 및 광배근 유리피판술을 받은 전력이 있는 케이스로 좌측 하악 견치와 제1,2소구치의 치성 감염을 원인으로 경부에서 상방으로 안와부위까지 파급된 두경부 괴사성 근막염 증례를 보고하는 것이다. 초진 시 국소 농양으로 판단되어 절개 및 배농술이 계획되었으나, 감염이 급속히 진행하여 광범위한 조직 괴사와 합병증이 발생하였다. 이에 반복적인 수술적 절제와 음압 창상치료요법(vacuum-assisted closure), 재건술을 통해 치료한 과정을 공유함으로써, 치성 감염에서 기원하여 안와 부위까지 확산된 드문 두경부 괴사성 근막염의 정확한 진단과 조기 치료 전략의 중요성을 강조하고자 한다.
증례
62세 남환이 3일 전부터 발생한 좌측 안면 종창과 입술 감각 저하를 주소로 본원 응급실에 내원하였다. 기저질환으로 당뇨병이 있었으며, 과거력에서 우측 하지에 발생한 괴사성 근막염으로 절개 및 배농술, 광배근 유리피판술을 수술받은 병력이 있었다. 내원 당시 좌측 하악각(mandibular angle)에서 악하(submandibular area)부위에 이르는 종창과 발적이 관찰되었다. 활력징후는 혈압 135/82 mmHg, 맥박수 122회/분, 호흡수 20회/분, 체온 37.8℃, 산소포화도 99%였다. 혈액검사에서는 백혈구 20.0 ×10³/μL, 호중구 84.5%(정상 40~75%), ESR 88 mm/hr(정상 0~10 mm/hr), CRP 270 mg/L(정상 0~5 mg/L)로 확인되었다. 조영증강 경부 전산화단층촬영(computed tomography; CT)에서는 좌측 악하부, 내·외측 익돌하악부(pterygomandibular space), 교근 및 인두주위(massteric and parapharyngeal space) 공간에 농양 소견이 관찰되었다(Fig. 1).
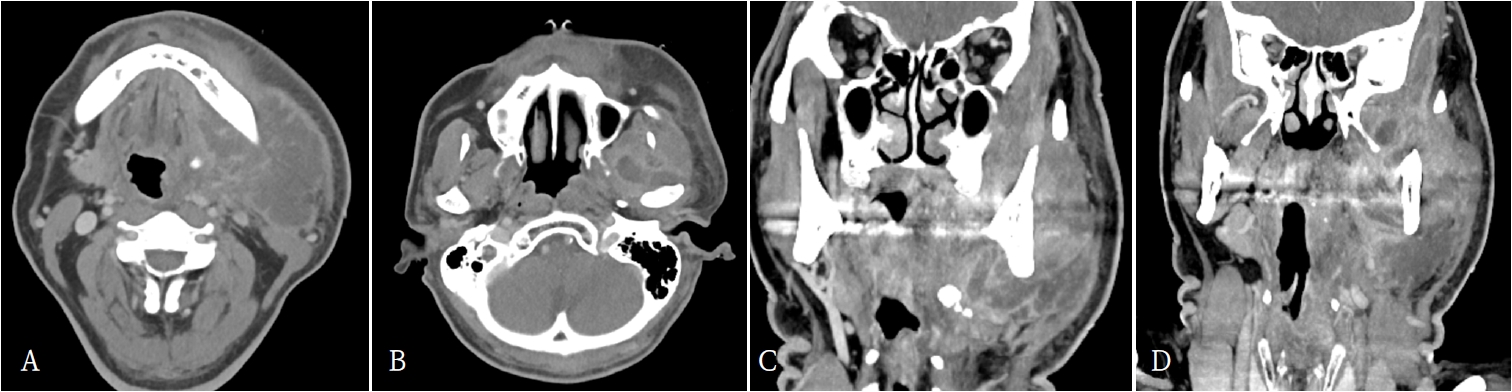
Contrast-enhanced neck computed tomographic images reveal abscess formation in the left submandibular space, pterygoid space (both medial and lateral), masseteric space, and parapharyngeal space. A and B. axial views, C and D. coronal views
국소마취 하 구강 내 및 구외 접근을 통한 절개 및 배농술을 시행하였으며, 항생제 정주 및 주기적 소독과 관류를 병행하였다. 초진 시 검사에서 HbA1c는 8.1%였으며, 식후 혈당은 200 mg/dL 이상으로 측정되었다. 이에 내분비내과와의 협진 하에 혈당 조절을 시행하였다. 치료 목표는 공복 혈당 80–120 mg/dL, 식후 혈당 <180 mg/dL로 설정하였으며, 이를 위해 Lantus 10 units, linagliptin 5 mg 1일 1회, metformin 500 mg 1일 1회를 투여하였다. 내원일부터 10일간 flomoxef 1g IV q12hr와 metronidazole 0.5g IV q8hr를 투여하였고, 배농된 농양에서 Klebsiella pneumoniae가 검출되었다. 그러나 입원 4일째 좌측 협부에 누공이 발생하였고, 이후 급속히 주변 연조직으로 감염이 파급되면서 광범위한 피부 및 근막의 괴사의 진행이 관찰되었다(Fig. 2).

A. Formation of a fistula in the left buccal and mandibular regions, B. Progressive replacement of viable tissue with necrotic tissue over time
이에 수차례 국소마취 및 진정요법 하에 괴사 조직 제거와 음압 창상치료요법 드레싱을 시행하였으나, 상태 호전이 미미하여 입원 3주차에 전신마취 하 광범위한 절제술 및 농양 배농술을 추가로 시행하였다(Fig. 3). 이후 감염내과 협진 하에 적절한 항생제 치료와 면밀한 추적관찰을 지속하였고, 전신마취 수술 직후부터 항생제는 piperacillin/tazobactam 4g q6hr로 변경하였다. 입원 4주차에는 괴사 진행의 정체 및 혈액학적 지표의 호전을 확인하였다. 이에 하악 하 부위에는 부분층 피부이식(split-thickness skin graft)을, 좌측 협부 및 하악하, 관골 부위에는 유경 대흉근 피판술(pectoralis major flap)을 통한 재건을 시행하였다(Fig. 4). 수술 과정에서 좌측 심부 측두부와 안와 주위(periocular)에서 추가 괴사 조직이 확인되어, 이를 충분히 세척하고 괴사 조직을 제거하였다. 이후 1주일뒤, 환자에서 안와 주위의 지속적인 종창 소견이 관찰되었으며 영상검사에서 안와 주위 농양(pus collection)이 확인되었다(Fig. 5). 이에 안과 협진 하에 전신마취 하 수술을 시행하였다. 수술 접근은 눈꺼풀주름 절개(lid crease incision) 및 상안와 접근(supraorbital approach)을 통해 이루어졌으며, 수술 중 대량의 농이 배액되었다. 농 및 조직은 배양검사를 위해 채취되었고, 괴사된 안와 중격(orbital septum), 골막(periosteum), 누선(lacrimal gland)을 절제하였다. 재건 부위는 양호한 치유를 보였으며, 환자는 퇴원 후 외래 추적관찰 중 재발 소견 없이 회복되었다(Fig. 6). 이후 괴사성근막염의 치성원인으로 판단되는 좌측 하악 견치, 제1소구치, 제2소구치의 근관치료를 진행하였다.
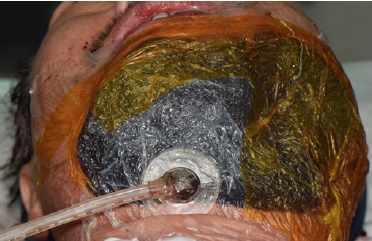
A. Wound management with vacuum-assisted closure therapy B. Wide excision and abscess drainage performed under general anesthesia

A. Procedure of pectoralis major flap elevation, B. Harvest of split-thickness skin graft. C. Completion of pectoralis major flap and split-thickness skin graft
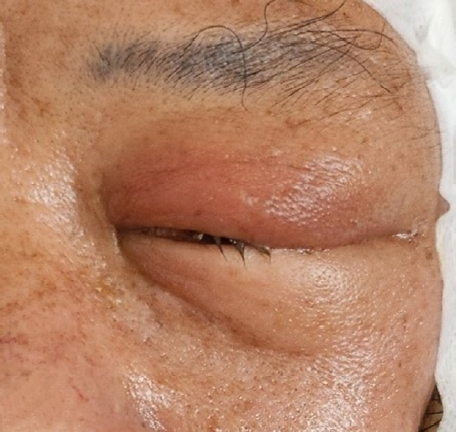
A. Clinical photograph demonstrates left periorbital swelling and eyelid edema, Increased extent of presumed abscess in left superolateral orbital cavity, leading to exophalmos. B. Axial view. C. Coronal view.
고찰
본 증례는 당뇨병을 기저질환으로 가진 환자에서 좌측 하악 견치 및 제1,2소구치의 치성 감염을 원인으로 발생한 경부를 포함한 안면부 괴사성 근막염으로, 초기 국소 농양으로 판단되어 절개 및 배농술 및 광범위 항생제 치료를 시작했으나 단기간에 급속한 연부조직 괴사가 진행된 증례이다. 본 증례의 특징적인 점은 감염이 경부 및 안면부를 넘어 안와 주위까지 확산되었다는 것이다. 치성 감염에 기인한 두경부 괴사성 근막염의 진행 중 발생한 이차적 안와 침범은 극히 드문 합병증으로, 문헌에 따르면 안와 주위 감염은 빠른 파급으로 인해 시력 소실, 안구 운동 장애, 심한 경우 두개 내 합병증으로까지 이어질 수 있다[11]. 본 증례에서는 좌측 경부, 협부 및 관골부위의 괴사와 더불어, 추가적으로 심부 측두부와 안와 주위에서 괴사 조직과 농양이 발견되었으며, 이후 안과적 접근(lid crease incision, supraorbital approach)을 통해 농 배액과 괴사 조직 제거가 시행되었다. 이는 치성 기원의 감염이 해부학적 공간을 따라 상방으로 확산될 수 있음을 보여주는 예로, 조기 영상검사와 다학제적 협진이 없었다면 심각한 합병증으로 이어질 수 있었을 것이다. 따라서 치성 감염으로 인한 괴사성 근막염 환자에서 안면부 및 안와 주위의 종창이 동반되는 경우, 안와 파급 가능성을 염두에 두고 적극적인 영상평가와 신속한 외과적 개입이 필요하다[12]. 조영증강 CT는 광범위 근막 비후, 근막면 액체 저류, 다공간 농양, 피하 기종 등 특징적 소견을 통해 병변 범위를 빠르게 가시화할 수 있어 1차 선택 영상으로 권고된다. 본 증례에서도 조영증강 CT가 병변의 다공간 침범을 확인하는 데 결정적이었다. 또한 Laboratory Risk Indicator for Necrotizing Fasciitis(LRINEC) 점수는 괴사성 근막염을 조기 감별하기 위해 고안된 검사실 기반 점수 체계로, WBC, CRP, Hb, Na, creatinine, glucose 등을 합산해서 점수를 내고, 6점 이상이면 괴사성 근막염 가능성이 높다고 해석한다. LRINEC 점수는 조기 선별에 도움을 줄 수 있으나 민감도 한계가 지적되어 임상 판단·영상 소견과 함께 해석해야 한다. LRINEC 점수 6점 이상은 괴사성 근막염을 강력히 시사하며, 8점 이상은 높은 특이도를 가지는 것으로 알려져 있다 13,14) . 본 증례에서 환자는 초진 내원 시 CRP 270 mg/L, 백혈구 20.0 ×10³/µL, 혈청 나트륨 132 mmol/L, 크레아티닌 1.17 mg/dL, 혈색소 15.1 g/dL, 혈당 230 mg/dL을 보였다. 이를 LRINEC 점수 체계에 적용하면 총 8점(CRP 4점, WBC 1점, Hb 0점, Na 2점, Creatinine 0점, Glucose 1점)으로 계산된다.
미생물학적으로 경부 괴사성 근막염은 혼합균 감염이 흔하나, 당뇨 등 대사성 질환 동반 시 Gram-negative 병원체의 관여 비율이 높아질 수 있다. 본 증례의 배양에서 Klebsiella pneumoniae가 동정되었는데, 최근 안면·경부 괴사성 근막염에서 K. pneumoniae가 임상적으로 유의미한 원인균으로 보고되는 사례가 늘고 있으며, 특히 당뇨 환자에서 치명률 증가와 연관될 수 있음이 지적된다. 이러한 근거는 초기 경험적 항생제 선택 시 광범위 그람음성·혐기성 커버리지의 필요성을 뒷받침한다[15,16]. 치료 원칙은 지체 없는 광범위 절제와 광범위 항생제의 병행이다. 경험적 항생제는 광범위 β-lactam/β-lactamase inhibitor(예: piperacillin/tazobactam) 또는 독소억제 목적의 clindamycin 등을 고려하고, 배양·감수성 결과에 따라 조정한다[17]. 본 증례에서 초기 flomoxef+metronidazole 후, 진행기에 piperacillin/tazobactam으로 조정한 전략은 이러한 권고와 부합한다[18]. 상처 관리 측면에서 음압 창상치료요법은 삼출물 제거, 부종 경감, 육아조직 유도, 상처 수축을 통해 감염 조절과 재건 전 준비에 유용할 수 있다. 경부 및 두경부 괴사성 근막염의 연속 증례와 최근 보고들은 음압 창상치료요법이 절제 범위와 드레싱 부담을 줄이고 상처 치유를 촉진할 수 있음을 시사한다[19]. 본 환자 역시 반복 절제와 음압 창상치료요법을 병행해 감염 부하를 낮춘 후, split-thickness skin graft와 대흉근 피판으로 단계적 재건을 시행해 양호한 결과를 얻었다. 다만 근거는 주로 증례·후향적 자료에 기반하므로, 적용 시 적절한 변연절제의 선행과 다학제 모니터링이 전제되어야 한다[20]. 보조요법으로의 고압산소치료(hyperbaric oxygen therapy)는 조직 산소분압을 높여 독소 생성 억제·호중구 살균능 개선·상처 치유 촉진을 도모할 수 있으나, 연구 간 예후의 이질성이 커 여전히 논쟁점이 있다. 최근 메타분석 및 대규모 코호트에서는 사망률 감소와 기능적 결과 개선 신호가 보고되지만, 비용·입원 기간 증가 등 교환관계가 존재하므로 시설·자원·환자 상태를 종합해 선별적으로 고려해야 한다[21]. 본 증례에서는 고압산소치료 없이도 반복 절제, 음압 창상치료요법, 재건으로 감염을 제어하였다.
본 증례의 환자는 과거 하지 괴사성 근막염의 수술력이 있었고, 이후 두경부 괴사성 근막염이 발생했다는 점에서 개체의 유전적 소인 가능성을 임상적으로 시사한다. 본 환자는 과거 하지 괴사성 근막염으로 광배근 피판 수술을 시행받은 병력이 있고 수년 후 두경부에서도 괴사성 근막염이 발생하였다. 최근 보고에 따르면 NFKB1 절단 변이 등 선천면역 조절 유전자 변이가 괴사성 근막염 발생 소인으로 작용할 수 있으며, HLA class II 대립유전자(HLA-DQA1) 또한 침습성 질환의 개체 감수성에 관여할 수 있다[22]. 이러한 문헌 근거는 동일 개인에서의 재발, 다부위 괴사성 근막염에 대해 유전적 소인을 임상적으로 의심할 근거를 제공한다.
종합하면, 치성 기원의 경부를 포함한 안면부 괴사성 근막염은 드물지만 진단 지연 시 치명률이 높은 응급질환이다. 본 증례는(Fig. 1), 위험인자(당뇨, 고염증 지표), 조영 증강 CT 기반 신속한 병기 평가, 반복적이고 충분한 절제 및 배농, 광범위 항생제의 적시 조정 음압 창상치료요법을 포함한 체계적 상처 관리 감염 안정화 이후 단계적 재건, 혈당의 엄격한 조절이라는 일련의 전략이 기능적 회복과 재발 방지에 기여함을 보여준다. 이러한 표준화된 접근과 다학제 협진 체계는 경부를 포함한 안면부 괴사성 근막염 환자의 예후 개선에 필수적이다.
Notes
Conflicts of Interest
None

